Estudio randomizado controlado con simulación: Este ensayo no mostró una reducción significativa de la presión arterial sistólica en los pacientes con hipertensión resistente.
Autor(es): Deepak L. Bhatt, M.D., M.P.H., David E. Kandzari, M.D., William W. O'Neill, M.D.,y cols.
Enlace: N Engl J Med 2014; 370:1393-1401
|
Antecedentes
Debido al envejecimiento de la población y a las crecientes tasas de obesidad, la hipertensión arterial está aumentando en todo el mundo1. Aproximadamente el 10 % de los pacientes con hipertensión diagnosticada tienen hipertensión resistente, definida como una presión arterial sistólica de 140 mm Hg o mayor a pesar de la adhesión a un régimen de tratamiento de al menos tres dosis máximas toleradas de medicamentos antihipertensivos de clases complementarias, incluyendo un diurético en una dosis apropiada1-4
Los pacientes con hipertensión resistente que están recibiendo tratamiento médico adecuado suelen tener altas tasas de complicaciones cardiovasculares, con pocas opciones de tratamiento.
El sistema nervioso simpático - en particular los vínculos entre los riñones y el cerebro - parece jugar un papel importante en la hipertensión resistente5 En una época anterior, los estudios no aleatorios mostraron que la simpatectomía quirúrgica es un tratamiento eficaz para algunos pacientes con hipertensión resistente, pero se registraron casos de hipotensión ortostática profunda después del procedimiento lo que hizo que esa terapéutica cayera en obsolescencia.6 ,7
Estudios anteriores “no ciegos” han sugerido que la denervación de la arteria renal con catéter reduce la presión arterial en pacientes con hipertensión resistente.
En los últimos años el tratamiento por catéter de radiofrecuencia de denervación de las arterias renales ha surgido como una alternativa posible para tratar la hipertensión arterial resistente y ya está en uso clínico en más de 80 países, incluyendo partes de Europa, América del Sur, Australia, y Canada.8-10
Estudios no aleatorizados iniciales y ensayos no ciegos aleatorios han demostrado grandes reducciones en la presión arterial, medida en una visita al consultorio, después de denervación renal11, 12
Sin embargo, varias limitaciones de estos estudios, entre ellos los pequeños tamaños de las muestras, la evaluación limitada de la presión arterial ambulatoria, la falta de cegamiento y la falta de un procedimiento simulado como control, hacen que la aplicación amplia de sus resultados resulten poco fiables.
El estudio HTN-3 SYMPLICITY fue cuidadosamente diseñado para superar estas limitaciones metodológicas.13
Métodos
Se diseñó un ensayo prospectivo aleatorizado, ciego simple controlado por simulación. Los pacientes con hipertensión resistente severa fueron asignados aleatoriamente en una proporción 2:1 a someterse a la denervación renal o un procedimiento simulado.
Los pacientes con hipertensión arterial resistente severa fueron inscritos prospectivamente en el estudio. En la selección inicial, los pacientes debían tener una presión arterial sistólica de 160 mm Hg o más (promedio de tres mediciones en una visita de consultorio [en adelante, la presión arterial en la consulta] mientras el paciente estaba sentado) y que recibiera dosis máximas toleradas de tres o más medicamentos antihipertensivos de clases complementarias, una de las cuales tenía que ser un diurético en la dosis correcta.
No se permitieron cambios en la medicación antihipertensiva en las 2 semanas anteriores. Durante las siguientes 2 semanas, los pacientes registraron su presión arterial en su hogar por la mañana y la noche y llevaron un diario que indicaba su adhesión a la terapia médica.
A continuación, se realizó una visita de selección de confirmación, durante la cual se confirmó la presión arterial sistólica de 160 mm Hg o mayor, se documentó la adherencia a los medicamentos, y se llevó a cabo la automatización de la monitorización ambulatoria de la presión arterial de 24 horas para asegurar una presión arterial sistólica de 135 mm Hg o superior.
Los criterios de exclusión clínicas fueron: causas secundarias conocidas de hipertensión arterial y más de una hospitalización por una emergencia hipertensiva en el año anterior. Los criterios de exclusión anatómicos fueron estenosis de la arteria renal de más de 50%, aneurisma de la arteria renal, intervención previa de la arteria renal, múltiples arterias renales, una arteria renal de menos de 4 mm de diámetro, o un segmento tratable de menos de 20 mm de longitud.
Los pacientes se sometieron a una angiografía renal antes de la aleatorización. A los 6 meses, a los pacientes del grupo de control se les permitió cruzar a someterse a la denervación si todavía cumplían con los criterios de inclusión para el estudio.
Síntesis de la metodología
- Antes de la aleatorización, los pacientes recibían un tratamiento antihipertensivo estable que implicaba las dosis máximas toleradas de al menos tres fármacos, incluyendo un diurético.
- El criterio de valoración principal de eficacia fue el cambio en la presión arterial sistólica de consultorio a los 6 meses, un punto final secundario de eficacia fue el cambio en la presión arterial sistólica ambulatoria media en el monitoreo de 24 horas.
- El punto final primario de seguridad fue un compuesto de muerte, la enfermedad renal en etapa terminal, eventos embólicos que resultara en daño de órgano terminal, complicaciones renovasculares, o una crisis hipertensiva en 1 mes o nueva estenosis de la arteria renal de más del 70 % a los 6 meses.
Resultados
Un total de 535 pacientes fueron sometidos a la aleatorización.
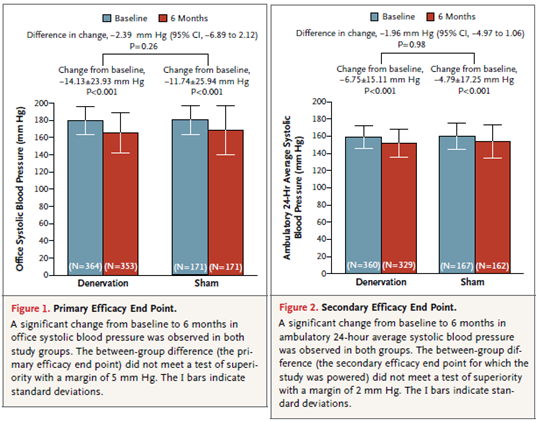
La media ( ± DE) del cambio en la presión arterial sistólica a los 6 meses fue de -14,13 ± 23,93 mm Hg en el grupo de denervación en comparación con -11,74 ± 25,94 mm Hg en el grupo de simulación de la cirugía (P < 0.001 para ambas comparaciones del cambio desde la línea de base ), para una diferencia de -2,39 mm Hg ( 95 % intervalo de confianza [ IC]: -6,89 a 2,12 , p = 0,26 para la superioridad con un margen de 5 mm Hg).
El cambio en las 24 horas de la presión arterial sistólica ambulatoria fue -6.75 ± 15.11 mm Hg en el grupo de denervación y -4.79 ± 17.25 mm Hg en el grupo de simulación de la cirugía, con una diferencia de -1,96 mmHg ( IC del 95 % , -4,97 a 1,06 , P = 0,98 para la superioridad con un margen de 2 mm Hg).
Discusión
Este estudio controlado por simulación, ciego y aleatorizado no mostró un beneficio de la denervación de la arteria renal en relación con cualquiera de los criterios de valoración de eficacia para los que el estudio fue diseñado (reducción de la presión arterial sistólica ambulatoria a los 6 meses en consultorio o ambulatoria).
Estos resultados contradicen los datos clínicos publicados con respecto a la denervación renal, que mostró mayores reducciones en la presión arterial 6 meses después de la denervación y, los del ensayo no cegado SYMPLICITY HTN– 2 sin reducción de la presión arterial sistólica en pacientes del grupo control 8,9,16.
El ensayo actual pone de relieve la importancia de la realización de ensayos cegados con controles simulados en la evaluación de nuevos dispositivos médicos antes de su adoption clínica18.
Hay varias explicaciones posibles para la discrepancia entre nuestros resultados y los resultados de la anterior estudios de denervación renal 11,12.
Estudios no aleatorizados previos compararon los resultados del tratamiento con las observaciones iniciales, más que con los resultados de un grupo de control, lo que lleva a una falsa impresión de la eficacia del tratamiento.
La regresión a la media puede haber estado en el juego de tal manera que los pacientes que tenían una presión arterial sistólica elevada en el día en que fueron reclutados en el ensayo pueden haber tenido una valoración posterior más baja, lo que indica una reducción que en realidad era un artefacto de los criterios de inclusión del estudio en relación con su presión arterial sistólica19.
Además, sin un grupo de control, el efecto del tratamiento observado pudo haber sido el resultado de la propia participación en ensayos clínicos con la reducción de la presión arterial sistólica, debido a una buena atención y a un alto grado de adherencia al tratamiento antihipertensivo, como resultado de un seguimiento más estrecho (efecto Hawthorne ). 20,21
Un ensayo aleatorio previo incluyó un grupo de control, pero la falta de cegamiento podría haber introducido un sesgo. Tanto los pacientes como los evaluadores pueden estar sujetos a un sesgo a favor de un nuevo tratamiento que se espera que tenga una mayor eficacia. La atribución errónea de un efecto placebo como un efecto del tratamiento es una limitación probable de esos estudio anteriores.22, 23
Nuestro análisis reveló que un efecto placebo importante estaba presente. Tal vez este efecto placebo fue acentuado por el uso de un procedimiento invasivo en el grupo de control (es decir, una punción de la arteria femoral y la angiografía renal), que pueden haber aumentado la adhesión a la medicación y la dieta. En cualquier caso, este hallazgo tiene importantes implicaciones terapéuticas para el diseño de los ensayos de antihipertensivos (y otros) medicamentos, dispositivos y estrategias.
Una limitación de este estudio es que la adherencia a la medicación no se pudo confirmar. Se sabe que más del 50 % de los pacientes con hipertensión arterial resistente no son adherentes a la medicación24
Aunque nosotros no medimos los niveles en orina de los medicamentos antihipertensivos, los pacientes tenían instrucciones específicas de seguir tomando sus medicamentos antihipertensivos en las dosis actuales, y el uso de medicamentos fue documentado durante un período de 2 semanas en los diarios antes de la línea de base del ensayo y antes de los 6 meses de la visita de seguimiento. No se encontraron pruebas de una diferencia significativa en la adherencia a la medicación entre los grupos.
Los cambios en la medicación entre las visitas de cribado pueden haber causado la inestabilidad de la presión arterial basal, pero sólo 31 pacientes (5,8 %) tuvieron un cambio de medicación durante este período, sin diferencia significativa entre los grupos en la presión arterial en la consulta en las visitas de cribado. Lo ideal hubiera sido medir la presión arterial por la mañana según lo recomendado por la American Heart Association.25 Aunque la presión arterial no siempre se midió por la mañana, se midió en aproximadamente el mismo tiempo, tanto en el inicio del estudio como en el seguimiento a los 6 meses.
El período de 6 meses desde el inicio hasta la determinación de punto final primario podría ser demasiado corto si un efecto placebo disminuyó con el tiempo, aunque los estudios anteriores mostraron un gran efecto a los 6 meses (que se mantuvo hasta 3 años), y los pacientes de nuestro estudio serán seguidos por un máximo de 5 años, incluyendo los que no se cruzan.
El ensayo no fue diseñado para detectar pequeñas diferencias en la presión arterial sistólica o diastólica, o cualquier efecto potencial en subgrupos. La curva de aprendizaje del operador puede afectar el éxito de los procedimientos de intervención, aunque fueron supervisados todos los procedimientos.
No observamos diferencias significativas en los resultados entre los operadores que realizaron cinco o más procedimientos y los que realizaron menos de cinco procedimientos, y no se encontraron pruebas de una curva de aprendizaje para los operadores de alto volumen cuando los procedimientos anteriores se compararon con los posteriores.
No había ninguna medición directa para confirmar que los nervios renales eran de hecho denervados por el procedimiento, porque no hay ninguna prueba de que se puede realizar fácilmente en un ensayo grande. Sin embargo, el sistema de catéter Symplicity permitió la confirmación de la entrega de energía, y la presencia de muescas angiográficas indicaron un efecto biológico sobre la arteria.
Por último, los resultados de este ensayo son específicos para el catéter probado y pueden no necesariamente ser generalizados a otros sistemas de denervación. La denervación renal en el ensayoactual parece ser segura, sin efectos secundarios imprevistos. Sin embargo, no se observó un efecto significativo sobre la presión arterial asistólica.
Conclusión
Este ensayo ciego no mostró una reducción significativa de la presión arterial sistólica en los pacientes con hipertensión resistente 6 meses después de la denervación de la arteria renal en comparación con un grupo control simulado.
Artículos relacionados
Referencias bibliográficas
1. Sarafidis PA, Georgianos P, Bakris GL. Resistant hypertension -- its identification and epidemiology. Nat Rev Nephrol 2013;9:51-58[Erratum, Nat Rev Nephrol 2013;9:492.]
2. Kumbhani DJ, Steg PG, Cannon CP, et al. Resistant hypertension: a frequent and ominous finding among hypertensive patients with atherothrombosis. Eur Heart J 2013;34:1204-1214
3. Smith SM, Gong Y, Handberg E, et al. Predictors and outcomes of resistant hypertension among patients with coronary artery disease and hypertension. J Hypertens 2013;32:635-643
4. Calhoun DA, Jones D, Textor S, et al. Resistant hypertension: diagnosis, evaluation, and treatment -- a scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research. Hypertension 2008;51:1403-1419
5. Bakris G, Nathan S. Renal denervation and left ventricular mass regression: a benefit beyond blood pressure reduction? J Am Coll Cardiol 2013 November 25 (Epub ahead of print).
6. Smithwick RH, Thompson JE. Splanchnicectomy for essential hypertension; results in 1,266 cases. J Am Med Assoc 1953;152:1501-1504
7. Grimson KS, Orgain ES, Anderson B, Broome RA, Longino FH. Results of treatment of patients with hypertension by total thoracic and partial to total lumbar sympathectomy, splanchnicectomy and celiac ganglionectomy. Ann Surg 1949;129:850-871
8. Bhatt DL, Bakris GL. The promise of renal denervation. Cleve Clin J Med 2012;79:498-500
9. Thukkani AK, Bhatt DL. Renal denervation therapy for hypertension. Circulation 2013;128:2251-2254
10. Myat A, Redwood SR, Qureshi AC, et al. Renal sympathetic denervation therapy for resistant hypertension: a contemporary synopsis and future implications. Circ Cardiovasc Interv 2013;6:184-197
11. Krum H, Schlaich M, Whitbourn R, et al. Catheter-based renal sympathetic denervation for resistant hypertension: a multicentre safety and proof-of-principle cohort study. Lancet 2009;373:1275-1281
12. Esler MD, Krum H, Sobotka PA, Schlaich MP, Schmieder RE, Bohm M. Renal sympathetic denervation in patients with treatment-resistant hypertension (the SYMPLICITY HTN-2 Trial): a randomised controlled trial. Lancet 2010;376:1903-1909
13. Kandzari DE, Bhatt DL, Sobotka PA, et al. Catheter-based renal denervation for resistant hypertension: rationale and design of the SYMPLICITY HTN-3 Trial. Clin Cardiol 2012;35:528-535
14. James KE, Bloch DA, Lee KK, Kraemer HC, Fuller RK. An index for assessing blindness in a multi-centre clinical trial: disulfiram for alcohol cessation -- a VA cooperative study. Stat Med 1996;15:1421-1434
15. Staessen JA, Wang JG, Thijs L. Cardiovascular protection and blood pressure reduction: a meta-analysis. Lancet 2001;358:1305-1315[Erratum, Lancet 2002;359:360.]
16. Esler MD, Krum H, Schlaich M, Schmieder RE, Bohm M, Sobotka PA. Renal sympathetic denervation for treatment of drug-resistant hypertension: one-year results from the SYMPLICITY HTN-2 randomized, controlled trial. Circulation 2012;126:2976-2982
17. Howard JP, Nowbar AN, Francis DP. Size of blood pressure reduction from renal denervation: insights from meta-analysis of antihypertensive drug trials of 4,121 patients with focus on trial design: the CONVERGE report. Heart 2013;99:1579-1587
18. Leon MB, Kornowski R, Downey WE, et al. A blinded, randomized, placebo-controlled trial of percutaneous laser myocardial revascularization to improve angina symptoms in patients with severe coronary disease. J Am Coll Cardiol 2005;46:1812-1819
19. Barnett AG, van der Pols JC, Dobson AJ. Regression to the mean: what it is and how to deal with it. Int J Epidemiol 2005;34:215-220
20. McCambridge J, Witton J, Elbourne DR. Systematic review of the Hawthorne effect: new concepts are needed to study research participation effects. J Clin Epidemiol 2014;67:267-277
21. Gale EA, Beattie SD, Hu J, Koivisto V, Tan MH. Recruitment to a clinical trial improves glycemic control in patients with diabetes. Diabetes Care 2007;30:2989-2992
22. Vaclavik J, Sedlak R, Plachy M, et al. Addition of Spironolactone in Patients with Resistant Arterial Hypertension (ASPIRANT): a randomized, double-blind, placebo-controlled trial. Hypertension 2011;57:1069-1075
23. Bakris GL, Lindholm LH, Black HR, et al. Divergent results using clinic and ambulatory blood pressures: report of a darusentan-resistant hypertension trial. Hypertension 2010;56:824-830
24. Jung O, Gechter JL, Wunder C, et al. Resistant hypertension? Assessment of adherence by toxicological urine analysis. J Hypertens 2013;31:766-774
25. Pickering TG, Hall JE, Appel LJ, et al. Recommendations for blood pressure measurement in humans and experimental animals: part 1: blood pressure measurement in humans: a statement for professionals from the Subcommittee of Professional and Public Education of the American Heart Association Council on High Blood Pressure Research. Circulation 2005;111:697-716



No hay comentarios:
Publicar un comentario