Experiencia actual en la hemorragia post pancreatectomía
Su manejo: Este estudio reporta la incidencia, manejo y resultados, en los últimos 5 años, de la hemorragia post pancreatectomía en un centro asistencial especializado en páncreas con un alto volumen de pacientes.
Dr. Correa-Gallego C, Brennan MF, D´Angelica M, DeMatteo RP, Fong Y, Kingham TP, Jarnagin WR, Allen PJ
J Am Coll Surg 2012; 215(5): 616-621
J Am Coll Surg 2012; 215(5): 616-621
Introducción
La hemorragia post pancreatectomía (HPP) es una complicación potencialmente letal de la resección pancreática [1,2]. Aunque menos común que la fístula pancreática postoperatoria o el retardo del vaciamiento gástrico, sigue siendo importante, con tasas reportadas entre el 6% y el 10% en la mayoría de las series [3-6]. Además, las tasas de mortalidad entre el 30% y el 50% subrayan la importancia de esta complicación, que es responsable de la mayoría de las muertes después de las resecciones pancreáticas en algunas series [7,8].
En el año 2007, el International Study Group of Pancreatic Surgery (ISGPS) propuso un sistema de clasificación que incluyó un sistema de gradación basado en el tiempo de comienzo, con 24 horas después de la finalización de la operación principal, como el límite entre hemorragia temprana y tardía; severidad, que consideró la magnitud de la caída de la hemoglobina y la necesidad de transfusión de sangre, así como los cambios hemodinámicos asociados; y localización del sangrado, intraluminal versus extraluminal [9]. Desde entonces se ha publicado un número de reportes integrando esa definición unificada [10-13].
Este estudio reporta la incidencia, manejo y resultados de la HPP en un centro pancreático con alto volumen de pacientes, en los últimos 5 años. La limitación a ese período de tiempo permite una evaluación precisa de las estrategias de manejo más actuales y sus resultados, dado que esos pacientes fueron tratados por el mismo grupo de profesionales. La definición del ISGPS fue aplicada a esa cohorte para evaluar su capacidad discriminatoria y significación pronostica.
Métodos
Se obtuvo la aprobación del comité de revisión institucional para examinar la base de datos, mantenida prospectivamente, de cirugía pancreática, del Memorial Sloan Kettering Cancer Center, en búsqueda de pacientes que hubieran sido sometidos a resección pancreática formal entre junio de 2006 y julio de 2011. Los datos de morbilidad se obtuvieron del programa Memorial Sloan Kettering Secondary Surgical Events, que es una plataforma para el registro en tiempo real de las complicaciones postoperatorias, auditada por cirujanos de planta y un equipo rotatorio de la casa, durante reuniones bisemanales de grupo [14]. Los datos fueron compilados en una base de datos segura de Microsoft Access. Las estadísticas descriptivas y comparativas fueron realizadas usando el programa SAS 9,2 (SAS Institute).
Pacientes
Los pacientes con sangrado gastrointestinal o hemorragia de cualquier grado de severidad en la base de datos del programa de Eventos Quirúrgicos Secundarios, fueron seleccionados para el análisis. Todos los datos clínicos y de laboratorio estuvieron disponibles en el sistema electrónico de registros médicos y el sistema de gradación del ISGPS fue aplicado retrospectivamente a esa cohorte. De acuerdo con las guías del ISGPS, la hemorragia severa fue definida como una pérdida de sangre de gran volumen (caída de la hemoglobina ≥ 3 g/dL), alteración hemodinámica clínicamente significativa (por ej., taquicardia, hipotensión, colapso cardiovascular), necesidad de transfusión de sangre o necesidad de tratamiento terapéutico invasivo. Los episodios de sangrado sin esas consecuencias fueron considerados leves. La hemorragia fue considerada intraluminal (intraentérica) cuando fue evidente, ya sea por hematemesis, salida de sangre por la sonda nasogástrica o por sangrado gastrointestinal bajo. La hemorragia extraluminal (extraentérica) se manifestó usualmente por salida de sangre por los drenajes intraperitoneales colocados quirúrgicamente o por una caída en el recuento sanguíneo y colapso cardiovascular, si no había drenajes colocados o habían sido removidos.
Recursos y dispositivos de radiología intervencionista
La institución de los autores tiene disponibilidad continua de radiología intervencionista propia, las 24 horas del día, los 365 días del año. En promedio, el tiempo desde la derivación hasta que el paciente está sobre la mesa (esto es, tiempo desde el sangrado hasta la aguja) es de aproximadamente 2 horas, Los dispositivos usados para el manejo endovascular de la HPP varían, dependiendo del origen de la hemorragia y de las características de los vasos sangrantes. Los coils de acero inoxidable son usado comúnmente para embolizar los vasos terminales, sin embargo, los stents recubiertos (por ej., VIABAHN de Gore) también son usados en el vaso sangrante, si la longitud del tronco no es ideal para la embolización y la permeabilidad distal de una rama de la vecindad es crítica (por ej., colocación de stent en el origen de la arteria gastroduodenal [AGD] preservando la permeabilidad en la arteria hepática propia).
Manejo de los datos y consideraciones estadísticas
El sexo, tipo de resección, consistencia pancreática, tamaño del conducto pancreático y del biliar, tipo de anastomosis entre el conducto pancreático y el biliar, control del remanente distal, uso de drenajes intraperitoneales, enfermedad maligna vs benigna y fístula pancreática concurrente (filtración o absceso intraabdominal), todos recolectados prospectivamente, fueron evaluados como predictores del desarrollo de HPP. En el modelo univariado, la p < 0,05 fue considerada significativa; aquellos factores con p ≤ 0,2 fueron incluidos en un modelo multivariado, comparando a los pacientes con y sin HPP para identificar los predictores de esa complicación. Las pruebas de chi-cuadrado, exacta de Fisher y de t , fueron usadas para la comparación de las variables categóricas y continuas, respectivamente. Los datos continuos son reportados como medianas y rangos intercuartilares (RIC), a menos que se especifique lo contrario.
Resultados
Se identificaron 1.122 pacientes que fueron sometidos a resección pancreática formal durante el período de 5 años de estudio. En una mediana del seguimiento alejado de 17 meses (rango, 7 a 32 meses), la HPP se desarrolló en 36 pacientes (3,2%). Se establecieron causas no relacionadas directamente con la resección pancreática en 3 pacientes y los mismos fueron excluidos del análisis; 2 pacientes tuvieron hemorragia como complicación de la colocación, guiada con radiología intervencionista, de catéteres para el drenaje de abscesos postoperatorios (laceraciones de arteria esplénica y de arteria torácica interna) y 1 paciente tuvo sangrado en la línea de engrampado de una anastomosis ileocólica que fue realizada sincrónicamente con una duodenopancreatectomía.
La incidencia de HPP fue del 3% (33 de 1.122). Los pacientes en los que se desarrolló la HPP fueron más jóvenes (59 años [rango 50 a 67] vs 66 años [rango 57 a 74]; p = 0,02) y el 54% fueron hombres (18 de 33). La mayoría había sido sometida a duodenopancreatectomía (25 de 33 [76%]), seguido por pancreatectomía distal (6 de 33 [18%]) y resecciones centrales (2 de 33 [6%]). Cuando se consideró la cohorte global, la incidencia de HPP no fue significativamente diferente entre esos procedimientos: 3% para la duodenopancreatectomía (25 de 739), 2% para la pancreatectomía distal (6 de 350) y 6% para las resecciones centrales (2 de 31) (p = 0,26).
Momento de aparición, ubicación y severidad
La hemorragia temprana (<24 hs después de la finalización de la operación principal) fue vista en el 21% (7 de 33 pacientes), todos los cuales se presentaron con sangrado extraluminal y manifestaciones clínicas severas de hipovolemia, Todos esos pacientes fueron sometidos a una reoperación urgente sin intentos diagnósticos o terapéuticos adicionales. Se encontró una hemostasia insuficiente y se la corrigió usando ligaduras y/o coagulación tisular en todos los casos.
Los restantes pacientes (26 de 33 [79%]) presentaron hemorragia tardía (>24 hs después de la finalización de la operación principal) a una mediana de 12 días postoperatorios (RIC 4 a 23 días). El 54% (14 de 26) de ese grupo tubo un sangrado severo, en contraste con el 100% del grupo de pacientes con hemorragia temprana (p < 0,01). La hemorragia tardía fue intraluminal en el 69% (18 de 26) de los pacientes y el 67% de los mismos (12 de 18) fue sometido a una endoscopía del tracto gastrointestinal superior en la presentación. La endoscopía permitió la identificación y el manejo de la fuente del sangrado en 3 de 12 pacientes (coagulación con plasma de argón o clips endoscópicos); se requirió evaluación y manejo angiográfico adicional en 3 de 12 (colocación de coils en un pseudoaneurisma de la arteria hepática, en una arteria hepática y en una AGD; ninguna de ellas tenia sangrado activo al momento de la arteriografía); los restantes 6 de 12 pacientes sin hallazgos durante la endoscopía se estabilizaron clínicamente y no necesitaron intervención adicional. De los pacientes con sangrado intraluminal que no fueron sometidos a una endoscopía alta (6 de 18), 4 se recuperaron clínicamente y no necesitaron intervención diagnóstica o terapéutica, 1 tuvo una angiografía con embolización de la AGD por un pseudoaneurisma y 1 se presentó con hemorragia en una institución diferente y falleció antes de que se instituyera el tratamiento; esa fue la única muerte en toda la cohorte.
El sangrado extraluminal ocurrió en el 31% (8 de 26) de los pacientes con hemorragia tardía y fue manejado de la siguiente manera: 3 fueron sometidos a re-exploración con control quirúrgico del sangrado en el 2º ó 3º día postoperatorio; la angiografía con embolización arterial se usó en 4 pacientes (2 AGD, 1 arteria esplénica y 1 rama polar superior de la arteria renal izquierda); y 1 tuvo un diagnóstico angiográfico sin evidencia de sangrado o pseudoaneurisma. Una comparación entre los pacientes con hemorragia temprana y tardía, su presentación y manejo, se resumen en la Tabla 1.
• TABLA 1: Datos demográficos, presentación clínica y resultados de 33 pacientes con hemorragia post pancreatectomía
.png)
El origen del sangrado para los 10 pacientes que fueron reoperados fue evaluado en un intento por identificar un patrón que pudiera guiar una inspección más estrecha y prevenir potencialmente esos eventos. Todos ellos tuvieron fuentes de sangrado que podían ser atribuidas a una hemostasia quirúrgica incompleta, esto es, sangrado del mesenterio del intestino delgado (n = 3), del muñón pancreático (n = 3), del lecho pancreático (n = 2), de la arteria epigástrica superior (n = 1) y de la curvatura menor arterial (n = 1).
De los predictores evaluados en el análisis univariado, la consistencia de la glándula (p = 0,09), tamaño del conducto pancreático (p = 0,07) tamaño del conducto biliar (p = 0,03) y fístula pancreática (p = 0,01) fueron incluidos en el análisis multivariado para evaluar los predictores del desarrollo de la HPP. Ninguno de esos factores estuvo significativamente asociado con el desarrollo de la HPP. Los pacientes con HPP tuvieron una mediana de estadía hospitalaria más alta (10 días [rango 8 a 17] vs 7 días [rango 6 a 8]; p < 0,01) que los pacientes sin esa complicación; no obstante, la mortalidad fue similar (1 de 33 [3%] vs 17 de 1.089 [2%]; p = 0,95).
La única muerte relacionada con la HPP ocurrió en un paciente dado de alta del hospital. Se presentó en otra institución in extremis con hematemesis masiva en el día 12º postoperatorio y, a pesar de un manejo óptimo, sucumbió a esa complicación poco después de su ingreso. En total, el 39% de los pacientes en esa cohorte (13 de 33) experimentaron su episodio de sangrado después del egreso inicial del hospital, con una mediana de 12 días (rango 7 a 20).
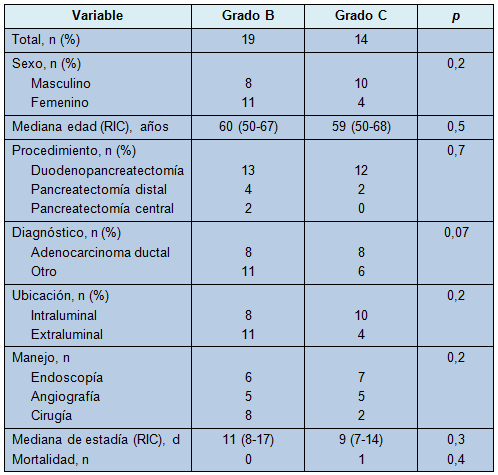
La clasificación del ISGPS para la HPP fue aplicada retrospectivamente y los grupos fueron comparados en términos de demografía, manejo y resultados. No hubo episodios de hemorragia de grado A, porque todos los pacientes con sangrado temprano tuvieron hemorragia severa y fueron re-explorados y, en consecuencia, fueron clasificados como grado B. No obstante, el manejo y los resultados de los pacientes con hemorragias de grado B y C fueron comparados y no se notaron diferencias entre esos grupos (Tabla 2).
TABLA 2: Datos demográficos, presentación clínica y resultados de los pacientes con HPP utilizando la clasificación del IGGPS
Discusión
Este estudio muestra que se puede alcanzar una baja mortalidad (3%) con el reconocimiento precoz y un manejo adecuadamente guiado de la HPP. Esto contrasta con la mayoría de los reportes previos que señalaron tasas de mortalidad a menudo tan altas como el 50% [7,8,15]. Existen varias explicaciones potenciales para estos resultados alentadores. Quizás el factor más importante responsable por la baja mortalidad en esta serie es el hecho de que este reporte incluye sólo a pacientes sometidos a resección desde el año 2006. La mayoría de las series publicadas reportan datos de cohortes desde comienzos de la década de 1990, cuando la angiografía percutánea y las intervenciones endoscópicas fueron usadas por primera vez y no estaban tan avanzadas y ampliamente disponibles como lo están hoy. Una larga proporción de pacientes en esa época requirió reoperación de una manera demorada con ligadura de pseudoaneurismas y/o terminación de la pancreatectomía, prácticas ambas que han sido abandonadas en la actualidad debido a sus resultados generalmente pobres [1,2,5,15,16].
Debido a esos hallazgos, el abordaje actual de los autores para el paciente que presenta una HPP más allá del período postoperatorio inmediato, es evitar – siempre que sea posible – la reoperación. Esos pacientes son sometidos a evaluación angiografía y endoscópica, dependiendo de la localización del sangrado (extra vs intraluminal) y el manejo adicional es dictado por los hallazgos de esos estudios y el estado hemodinámico general del paciente. En la presente serie, el manejo quirúrgico se usó sólo en los pacientes en el período postoperatorio temprano; en el 70% de aquellos sometidos a reoperación, se hizo dentro de las 24 horas de la operación principal, pero el 30% restante fue sometido a reoperación entre las 24 y las 72 horas después de la resección; todos esos pacientes tuvieron una recuperación sin contratiempos sin episodios recurrentes de sangrado. Los pacientes que se presentaron con hemorragia tardía fueron evaluados mediante angiografía intervencionista o endoscopía del tracto gastrointestinal superior; la primera fue terapéutica la mayoría de las veces (8 de 10 pacientes). En contraste, la endoscopía digestiva alta fue mayormente un instrumento diagnóstico, permitiendo un manejo terapéutico exitoso en sólo 3 de 13 pacientes. Otros grupos han publicado algoritmos para el manejo de las HPP [6,17,18] que son en su mayor parte comparables con los de los autores de este trabajo. La mayoría de esos reportes (incluyendo el actual) están limitados por su naturaleza retrospectiva y por la rareza de esta complicación y reflejan desvíos institucionales considerables. No obstante, los datos randomizados no están disponibles y probablemente nunca lo estarán, a causa de las limitaciones en el poder estadístico y la falta de estabilidad clínica.
Sangrado centinela
Cerca de 20 años atrás, el término “sangrado centinela” fue acuñado en referencia a episodios leves de sangrado, que fueron siendo cada vez más reconocidos como estrechos predictores de una hemorragia mayor [1,2,19]. En un reciente meta-análisis, ese signo de alarma se encontró en aproximadamente el 33% de las veces [7]; sin embargo, sólo la mitad de las publicaciones (9 de 20) consideraron que ese estudio había reportado episodios de sangrado centinela. En un estudio prospectivo publicado en 2008 por Tien y col. [20], todos los pacientes con sangrado centinela (definido como la aparición o incremento en la cantidad de sangre por los drenajes abdominales o en el tracto gastrointestinal y una caída en la hemoglobina > 2 gr/dL, 3 días después de la pancreatectomía) fueron sometidos a angiografía. Identificaron y realizaron angiografía en 20 pacientes, descubriendo pseudoaneurismas en 7 pacientes que fueron exitosamente embolizados, sin sangrado adicional; los pacientes con angiogramas negativos tuvieron resultados variables: se desarrolló una hemorragia masiva en 3 de 13 pacientes, que requirió laparotomía de emergencia, 6 de 13 pacientes tenían úlceras marginales identificadas en la endoscopía y 4 de 13 pacientes no tuvieron una fuente identificada y no presentaron sangrado adicional.
Con las modernas alternativas mínimamente invasivas, diagnósticas e intervencionistas, a la cirugía, la evaluación completa y la intervención temprana son prácticas comunes en la actualidad, aun después de episodios menores de sangrado. A menudo, las grandes hemorragias subsiguientes, necesarias para definir a la primera como centinela, son evitadas. Muchas de las que habían sido consideradas hemorragias centinelas en el pasado, pueden ser clasificadas ahora como hemorragia leve tardía (o ISGPS grado B).
Aplicabilidad de la clasificación ISGPS
Hasta donde llega el conocimiento de los autores de este trabajo, se han publicado unos pocos estudios evaluando la definición del ISGPS. Rajarathinam y col., reportaron su experiencia con la hemorragia después de la duodenopancreatectomía en una cohorte de 458 pacientes, durante un período de 10 años [12]. La tasa de HPP en su serie fue del 3%, aunque sólo incluyeron casos de hemorragia severa que ocurrieron entre el 1º y el 40º día postoperatorio. Su cohorte fue dividida equitativamente entre grados B y C (7 pacientes en cada uno) y reportaron una mortalidad global del 29%. El manejo de esos pacientes fue primariamente quirúrgico (71%). En un estudio grande de Welsch y col., se encontró una incidencia muy alta de HPP (29%) cuando se aplicó loa definición del ISGPS; la gran mayoría de los pacientes (97%), no obstante, no tenía signos clínicos de sangrado y sólo el 4,6% requirió reintervención [13]. Aunque esos autores concluyeron que la definición era capaz de segregar pacientes en grupos con resultados diferentes y que era aplicable, el hecho de que una gran proporción de pacientes estuviera asintomática y que unos pocos requirieran reintervención, debería generar preocupación acerca de la sobresensibilidad de la clasificación actualmente recomendada. Grützman y col., reportaron su experiencia con 945 pacientes durante 16 años [11]; la HPP se desarrolló en el 5,7% de los mismos, siendo aproximadamente un tercio de grado B y dos tercios de grado C. Reportaron una mortalidad global del 26%, que no difirió significativamente entre los grados B y C (p = 0,07). La duración de la estadía en la unidad de cuidados intensivos y en el hospital, fue significativamente mayor en los pacientes con grado C (4,2 y 20 días vs 21 y 40 días; p < 0,05 para ambas).
La aplicación la clasificación ISGPS a la cohorte de los autores de este trabajo, no segregó a los pacientes en categorías de riesgo diferentes y no los diferenció en términos de manejo o resultados (Tabla 2). Los pacientes con HPP de grado A no fueron identificados, pero pudieron no haber sido capturados en la base de datos de morbilidad de los autores, porque esas hemorragias tempranas leves, por definición, son mayormente asintomáticas. Además, los resultados de este trabajo sugieren que el límite de 24 horas establecido en la definición del ISGPS (usado para este análisis), podría ser demasiado estricto y un intento de segregar pacientes con causas uniformes de sangrado puede requerir la inclusión de episodios que ocurren hasta las 72 horas postoperatorias.
Además, es concebible que hubo eventos de sangrado que ocurrieron después del egreso hospitalario que no fueron documentados, especialmente si los pacientes buscaron atención en instituciones diferentes. Sin embargo, el tiempo prolongado de seguimiento alejado de este estudio (17 meses) hace poco probable esa posibilidad, porque los autores indagaron rutinariamente sobre cualquier evento adverso después de la cirugía, cada vez que se estableció contacto con los pacientes y lo documentaron en su base de datos de complicaciones; no obstante, esta es una limitación potencial de este estudio.
Conclusiones
El manejo de la HPP debería estar individualizado y basado sobre un escenario clínico específico, causa presumida y disponibilidad de recursos. Como regla general, toda hemorragia severa es manejada mejor con re-exploración, dado que es probable hallar una causa de sangrado quirúrgicamente corregible. Por otro lado, el sangrado tardío debería ser agresivamente evaluado, ya sea con endoscopía digestiva alta o con angiografía y el manejo adaptado a la ubicación y gravedad.
Esta experiencia contemporánea muestra que la HPP sigue siendo una complicación rara pero grave después de la cirugía pancreática. Los resultados favorables y una mortalidad muy baja pueden alcanzarse con un abordaje agresivo para el diagnóstico y manejo de esos pacientes al momento de su presentación. Cirujanos, médicos y pacientes deberían tener conciencia del riesgo de la HPP que se presenta tardíamente (después del egreso) y de los mecanismos apropiados para una rápida derivación. La definición del ISGPS de la HPP brinda una definición común aplicable y un marco de trabajo para la comunicación entre cirujanos en todo el mundo; sin embargo, la experiencia de los autores, al igual que la de otros, origina preocupaciones por sobresensibilidad de la definición de la hemorragia leve.


No hay comentarios:
Publicar un comentario