Edema: ¿cómo abordarlo en la práctica? Un signo de consulta frecuente que responde a múltiples causas y requiere de una exploración sistemática y rigurosa.
Dres. Thomas Jefferson, Rutgers Robert Wood
Diagnosis and Management. American Family Physician 2013;88(2):102-110
Recibido vía hotmail de IntraMed, Traducción y resumen objetivo: Dra. Marta Papponetti
El edema es la acumulación de líquido en el tejido intercelular que proviene de la expansión anormal del volumen del líquido intersticial.
El líquido en los espacios intersticial e intravascular está regulado por el gradiente de la presión hidrostática capilar y el gradiente de la presión oncótica capilar. La acumulación del líquido ocurre cuando este equilibrio se altera por condiciones locales o sistémicas, provocando un aumento de la presión hidrostática capilar y del volumen plasmático, con disminución de la presión oncótica plasmática (hipoalbuminemia) y mayor permeabilidad capilar u obstrucción linfática.
Evaluación del edema
Historia
La historia debe incluir en qué momento aparece el edema, si se produce con los cambios de posición, si es unilateral o bilateral y también debe incluir datos sobre los medicamentos que recibe el paciente y las enfermedades sistémicas existentes.
La aparición aguda en una extremidad en un período <72 horas es más característica de la trombosis venosa profunda (TVP), la celulitis, la ruptura de un quiste poplíteo, el síndrome compartimental agudo postraumático o, el inicio reciente de un tratamiento con bloqueantes de los canales de calcio.
El edema crónico más generalizado se debe a la aparición o la exacerbación de enfermedades sistémicas crónicas, como la insuficiencia cardíaca congestiva (ICC), la enfermedad renal o la enfermedad hepática.
El edema de estasis causado por la insuficiencia venosa mejora con la elevación de las piernas y empeora con la posición péndula de las extremidades o con la estación de pie. El edema se asocia con la disminución de la presión oncótica del plasma (por ej., mala absorción, insuficiencia hepática, síndrome nefrótico) y no se modifica por la posición.
El edema unilateral por compresión o compromiso del drenaje venoso o linfático puede derivar de la TVP, la insuficiencia venosa, la obstrucción venosa (por ej., obstrucción tumoral de la vena ilíaca), la obstrucción linfática (por ej., a partir de un tumor pélvico o linfoma), o la destrucción linfática (por ej., congénita o secundaria a un tumor, radiación o filariasis).
La inflamación bilateral o generalizada sugiere una causa sistémica, como la ICC (sobre todo si es del lado derecho), hipertensión pulmonar, insuficiencia renal crónica o enfermedad hepática (causando hipoalbuminemia), enteropatías perdedoras de proteínas o desnutrición grave.
Tabla 1 . Causas de edema sistémicas y localizadas.(Ver tabla)
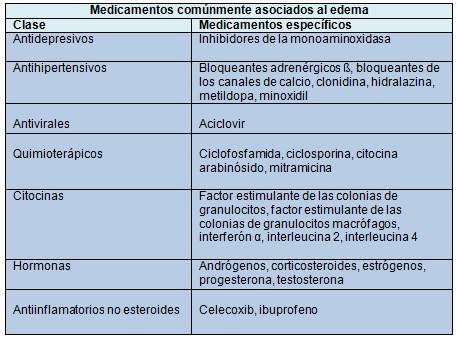
El edema puede ser un efecto adverso de ciertos medicamentos
El mecanismo incluye a menudo la retención de sal y agua con aumento de la presión hidrostática capilar. El uso de diuréticos puede causar depleción de volumen y la estimulación refleja del sistema renina-angiotensina.
Se debe interrogar acerca de enfermedades cardiacas, renales, tiroideas o hepáticas. La enfermedad de Graves puede provocar mixedema pretibial, mientras que el hipotiroidismo puede causar mixedema generalizado.
Aunque se considera un diagnóstico de exclusión, la apnea obstructiva del sueño puede causar edema. Un estudio evaluó el índice de apneas-hipopneas durante el sueño en pacientes con apnea obstructiva del sueño y encontró que incluso cuando se ajusta por la edad, el índice de masa corporal y la presencia de hipertensión y diabetes mellitus, dicho índice fue mayor en los pacientes que tenían edema.
Examen físico
El examen físico debe evaluar las causas sistémicas del edema, como la insuficiencia cardíaca (por ej., ingurgitación yugular, estertores crepitantes), la enfermedad renal (por ej., proteinuria, oliguria), enfermedad hepática (por ej., ictericia, ascitis, asterixis) o, enfermedad tiroidea (por ej., exoftalmos, temblor, pérdida de peso). También se debe evaluar si la piel presenta fóvea, dolor al tacto y cambios en la piel.
La fóvea se describe como un hoyuelo que permanece en la zona donde se ha ejercido presión, lo que ocurre cuando el líquido en el espacio intersticial tiene una baja concentración de proteínas, lo que se asocia a una disminución de la presión oncótica plasmática y a trastornos causados por el aumento de la presión capilar (por ej., TVP, ICC, compresión de la vena ilíaca). El médico debe describir el sitio, el momento y la magnitud de la fóvea, para determinar la respuesta al tratamiento. El examen de las extremidades inferiores se debe hacer en el maléolo interno, la porción ósea de la tibia, y el dorso del pie.
El edema con fóvea también se produce en las primeras etapas del linfedema, por afluencia de líquido rico en proteínas en el intersticio, antes de que se produzca la fibrosis del tejido subcutáneo, por lo tanto, su presencia no debe excluir el diagnóstico de linfedema.
La sensibilidad a la palpación sobre el área edematosa se asocia con TVP y el síndrome doloroso regional tipo 1 (distrofia simpática refleja). Por el contrario, en el linfedema, generalmente la palpación no provoca dolor. Los cambios en la temperatura de la piel, el color y la textura proporcionan pistas sobre la causa del edema.
Por ejemplo, la TVP aguda y la celulitis pueden producir aumento del calor sobre el área afectada. Debido a la deposición de hemosiderina, la insuficiencia venosa crónica suele ir acompañada por una piel bronceada oscura, rojiza, que comúnmente compromete a maléolo interno.
A medida que la insuficiencia venosa progresa puede producirse lipodermatoesclerosis, acompañada por tejido esclerótico y marcada hiperpigmentación, y caracterizada por fibrosis y deposición de hemosiderina, que puede conducir a úlceras venosas sobre el maléoto interno.
Estas úlceras pueden progresar hacia la profundidad, provocando erosiones importantes. El mixedema del hipotiroidismo presenta piel seca, gruesa, con edema periorbital que no deja fóvea y decoloración de la piel (amarilla a naranja en las rodillas, los codos, las palmas y las plantas).
El mixedema pretibial localizado puede estar ocasionado por la enfermedad de Graves. En las últimas etapas del síndrome de dolor regional complejo, la piel puede tener aspecto brillante con cambios atróficos. En las primeras etapas del linfedema, la piel tiene aspecto pastoso, mientras que en las etapas posteriores puede ser fibrótica, engrosada y verrugosa. En presencia de edema en las extremidades inferiores es importante examinar los pies. En los pacientes con linfedema no se puede tomar la piel del dorso del segundo dedo del pie utilizando una pinza de agarre (signo de Kaposi-Stemmer).
En los pacientes con lipedema, que es una acumulación patológica de tejido adiposo en las extremidades, generalmente los pies están respetados, aunque los tobillos suelen ser prominentes debido al depósito de grasa en los maléolos. El lipedema también puede afectar a las extremidades superiores.
Pruebas diagnósticas
Las siguientes pruebas de laboratorio son útiles para el diagnóstico de las causas sistémicas de edema: medición del péptido natriurético cerebral (para la ICC), medición de la creatininemia y análisis de orina (para las enfermedades renales), y medición de las enzimas hepáticas y albúmina plasmática para la enfermedad hepática.
En los pacientes que presentan edema unilateral en forma aguda, en una extremidad superior o inferior o en pacientes de bajo riesgo, la TVP puede ser descartada midiendo el D-dímero por enzimoinmunoensayo. Sin embargo, esta prueba tiene una especificidad baja y se pueden hallar concentraciones elevadas del dímero D en ausencia de trombosis.
Ecografía
La ecografía venosa es la técnica de imagen de elección para confirmar o descartar la TVP. La ecografía por compresión con o sin análisis de la onda Doppler tiene una sensibilidad y especificidad elevadas (95% y 96%, respectivamente) para la trombosis proximal, pero la sensibilidad es menor para las venas de la pantorrilla (73%). La ecografía Duplex también se puede utilizar para confirmar el diagnóstico de la insuficiencia venosa crónica.
Linfocentellografía
El flujo linfático no se puede detectar mediante la ecografía. Por lo tanto, la linfocentellografía indirecta con radionúclidos permite ver si hay ausencia o el retardo del llenado de los canales linfáticos y cuando el diagnóstico no se puede hacer en forma clínica es el método de elección para evaluar el linfedema.
Imágenes por resonancia magnética
Los pacientes con edema unilateral de las extremidades inferiores en los que no se ha comprobado la trombosis proximal por medio de la ecografía dúplex y siguen teniendo el diagnóstico presuntivo de TVP pueden requerir de la información que brindan las imágenes adicionales. Para evaluar la TVP intrínseca o extrínseca del muslo o la pelvis se puede utilizar la angiografía por resonancia magnética con venografía de la extremidad inferior y la pelvis.
La compresión de la vena ilíaca izquierda por la arteria ilíaca derecha (Síndrome de May-Thurner) debe sospecharse en las mujeres de 18 y 30 años que presentan edema de la extremidad inferior izquierda.
Las imágenes por resonancia magnética pueden ayudar al diagnóstico de enfermedades musculoesqueléticas (desgarro del gemelo, quiste poplíteo). Ante la sospecha de linfedema se puede utilizar la linfangiografía por resonancia magnética ponderada en T1, la que permite visualizar directamente los canales linfáticos.
Otros estudios
La ecocardiografía permite evaluar las presiones arteriales pulmonares y está recomendada para los pacientes con apnea obstructiva del sueño y edema.
En un estudio de pacientes con apnea del sueño obstructiva, el 93% de los pacientes con edema tienen presiones arteriales elevadas. Durante mucho tiempo se ha pensado que la hipertensión pulmonar derecha es la causa del edema asociado a la apnea obstructiva del sueño. Sin embargo, un estudio comprobó que a pesar de que una elevada proporción de pacientes con edema tenía apnea obstructiva del sueño (más de dos tercios), casi un tercio de estos pacientes no tenía hipertensión pulmonar, lo que pone de manifiesto una correlación estrecha entre el edema y la apnea obstructiva del sueño, que puede explicase por la presencia de la hipertensión pulmonar sola.
Manejo del edema
El manejo del edema depende de la etiología subyacente, la que comúnmente incluye la insuficiencia venosa crónica, el linfedema, la TVP y el edema secundario a medicamentos, entre otras.
Insuficiencia venosa cónica
En los pacientes con insuficiencia venosa crónica debe evitarse el tratamiento diurético a menos que exista una comorbilidad que lo requiera (por ej., ICC).
Para el edema leve, se utilizan tratamientos mecánicos, como la elevación de las piernas y el uso de medias compresivas con 20 a 30 mm Hg.
Para el edema grave complicado con ulceraciones, se recomiendan las medias con 30 a 40 mm Hg.
El tratamiento compresivo está contraindicado en los pacientes con enfermedad arterial periférica.
"Antes de prescribir el tratamiento compresivo en los pacientes con factores de riesgo de enfermedad arterial periférica se debe considerar la medición del índice tobillo-brazo"
Un estudio de 120 pacientes con úlceras venosas mostró que el 6% tenía úlceras arteriales y venosas. En otro estudio, las mujeres con síntomas de insuficiencia venosa crónica mostraron una mayor prevalencia de enfermedad arterial periférica que las mujeres asintomáticas. Por lo tanto, antes de prescribir el tratamiento compresivo en los pacientes con factores de riesgo de enfermedad arterial periférica se debe considerar la medición del índice tobillo-brazo.
Existe evidencia mixta para el uso de dispositivos de compresión neumática en los pacientes con la insuficiencia venosa crónica. Sin embargo, estos dispositivos pueden ser útiles para los pacientes en los que están contraindicadas medias compresivas.
Para la insuficiencia venosa crónica leve a moderada, un tratamiento alternativo o complementario de la terapia compresiva es el extracto de semillas de castaño de indias.
El cuidado de la piel local y de las úlceras venosas es muy importante para prevenir la celulitis y la dermatitis secundarias. En los pacientes con insuficiencia venosa crónica a menudo se produce dermatitis eczematosa (estasis), caracterizada por sequedad, inflamación y descamación de piel suprayacente a las venas varicosas superficiales. El tratamiento incluye la hidratación diaria con emolientes y cursos cortos de cremas con esteroides tópicos, en el caso de una piel severamente inflamada.
Linfedema
La base del tratamiento del linfedema es la fisioterapia descongestiva compleja compuesta por el masaje linfático manual y un vendaje multicapa. El objetivo inicial es mejorar la reabsorción del líquido hasta lograr la máxima respuesta terapéutica. La fase de mantenimiento del tratamiento incluye el uso de medias de compresión de 30 a 40 mm Hg.
Se ha demostrado que los dispositivos de compresión neumática mejoran el tratamiento estándar. Un ensayo aleatorizado controlado de mujeres con cáncer de mama y linfedema mostró una mejoría estadísticamente significativa de la función linfática tras una hora de tratamiento de compresión neumática.
En un estudio de 155 pacientes con cáncer y linfedema no relacionado con el cáncer, el 95% experimentó la reducción del edema de los miembros después de usar dispositivos de compresión neumática en su domicilio. Los procedimientos para reducir el volumen o la derivación quirúrgica se limitan a los casos refractarios graves. Los diuréticos no tienen un papel en el tratamiento del linfedema.
Trombosis venosa profunda
Los episodios trombóticos agudos se tratan con anticoagulantes (heparina no fraccionada de bajo peso molecular o warfarina) con el fin de prevenir la progresión de un coágulo o el desarrollo del síndrome postrombótico.
Este síndrome se caracteriza por la hinchazón crónica de las piernas, dolor, calambres y cambios en la piel, incluyendo telangiectasias, las que se producen en el 20% al 50% de los pacientes, dentro de los 5 años de un episodio de trombosis. Después de una TVP, además de la anticoagulación se deben usar medias compresivas para prevenir el síndrome postrombótico.
En una revisión de Cochrane de 2 estudios controlados aleatorizados que a los 2 años compararon el resultado de las medias elásticas de compresión (20 a 30 mm de Hg) con el placebo en pacientes con TVP, los pacientes que usaron medias de compresión mostraron una reducción estadísticamente significativa del riesgo de desarrollar un síndrome postrombótico.
Un estudio controlado aleatorizado de 209 pacientes con TVP proximal, a los 24 meses mostró que los pacientes sometidos a trombólisis dirigida por catéter complementando la terapia compresiva conservadora y el tratamiento anticoiagulante tuvieron una prevalencia más baja de síndrome postròmbótico, comparado con la terapia conservadora sola, lo que indica que la trombólisis puede ser un tratamiento opcional para pacientes seleccionados.
Edema provocado por medicamentos
Ante la sospecha de edema inducido por medicamentos, siempre que sea posible se debe suspender el fármaco sospechoso. En los pacientes que toman bloqueantes de los canales de calcio para el tratamiento de la hipertensión, el uso de un inhibidor de la enzima convertidora de angiotensina puede ser más beneficioso que el de los bloqueantes de los receptores de angiotensina, y puede reducir el edema periférico provocado por los bloqueantes de los canales de calcio.
Otras causas
No existe tratamiento para el lipedema. La pérdida de peso no mejora esta condición. El síndrome de dolor regional complejo se trata con fisioterapia combinada con esteroides sistémicos y antidepresivos tricíclicos. La apnea obstructiva del sueño puede tratarse con ventilación con presión positiva.
Referencias Bibliográficas
1. Braunwald E, Loscalzo J. Edema. In: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J, eds. Harrison’s Principles of Internal Medicine. 18th ed. New York, NY: McGraw-Hill; 2011.http://www.accessmedicine.com/content.aspx?aid=9097476. Accessed January 7, 2012.
2. O’Brien JG, Chennubhotla SA, Chennubhotla RV. Treatment of edema. Am Fam Physician. 2005;71(11):2111-2117.
3. Cho S, Atwood JE. Peripheral edema. Am J Med. 2002;113(7):580-586. 4. Yale SH, Mazza JJ. Approach to diagnosing lower extremity edema. Compr Ther. 2001;27(3):242-252.
5. Ely JW, Osheroff JA, Chambliss ML, Ebell MH. Approach to leg edema of unclear etiology. J Am Board Fam Med. 2006;19(2):148-160.
6. Warren AG, Brorson H, Borud LJ, Slavin SA. Lymphedema: a comprehensive review. Ann Plast Surg. 2007;59(4):464-472.
7. Tiwari A, Cheng KS, Button M, Myint F, Hamilton G. Differential diagnosis, investigation, and current treatment of lower limb lymphedema. Arch Surg. 2003;138(2):152-161.
8. Alguire PC, Mathes BM. Chronic venous insufficiency and venous ulceration. J Gen Intern Med. 1997;12(6):374-383.
9. Rockson SG. Lymphedema. Am J Med. 2001;110(4):288-295.
10. Rockson SG. Diagnosis and management of lymphatic vascular disease. J Am Coll Cardiol. 2008;52(10):799-806.
11. Rockson SG. Current concepts and future directions in the diagnosis and management of lymphatic vascular disease. Vasc Med. 2010;15(3):223-231.
12. Rudkin GH, Miller TA. Lipedema: a clinical entity distinct from lymphedema. Plast Reconstr Surg. 1994;94(6):841-847.
13. Kesieme E, Kesieme C, Jebbin N, Irekpita E, Dongo A. Deep vein thrombosis: a clinical review. J Blood Med. 2011;2:59-69.
14. Topham EJ, Mortimer PS. Chronic lower limb oedema. Clin Med. 2002;2(1):28-31.
15. Iftikhar I, Ahmed M, Tarr S, Zyzanski SJ, Blankfield RP. Comparison of obstructive sleep apnea patients with and without leg edema. Sleep Med. 2008;9(8):890-893.
16. Villeco JP. Edema: a silent but important factor. J Hand Ther. 2012;25(2):153-162.
17. Gorman WP, Davis KR, Donnelly R. ABC of arterial and venous disease. Swollen lower limb-1: general assessment and deep vein thrombosis [published correction appears in BMJ. 2000;321(7256):266]. BMJ. 2000;320(7247):1453-1456.
18. Brotman DJ, Segal JB, Jani JT, Petty BG, Kickler TS. Limitations of D-dimer testing in unselected inpatients with suspected venous thromboembolism. Am J Med. 2003;114(4):276-282.
19. Rose SC, Zwiebel WJ, Nelson BD, et al. Symptomatic lower extremity deep venous thrombosis: accuracy, limitations, and role of color duplex flow imaging in diagnosis [published correction appears in Radiology. 1990;176(3):879]. Radiology. 1990;175(3):639-644.
20. Kearon C, Julian JA, Newman TE, Ginsberg JS. Noninvasive diagnosis of deep venous thrombosis. McMaster Diagnostic Imaging Practice Guidelines Initiative [published correction appears in Ann Intern Med. 1998;129(5):425]. Ann Intern Med. 1998;128(8):663-677.
21. Studdiford J, Lamb K, Stonehouse A. Evaluating edema of the hands. J Musculoskel Med. 2009;26(1):30-36.
22. Wolpert LM, Rahmani O, Stein B, Gallagher JJ, Drezner AD. Magnetic resonance venography in the diagnosis and management of May-Thurner syndrome. Vasc Endovascular Surg. 2002;36(1):51-57.
23. American College of Radiology. ACR Appropriateness Criteria: suspected lower extremity deep vein thrombosis.http://gm.acr.org/SecondaryMainMenuCategories/quality_safety/app_criteria/pdf/Vascular/SuspectedLowerExtremityDeepVeinThrombosisDoc19.aspx. Accessed January 30, 2012.
24. Umeoka S, Koyama T, Togashi K, Kobayashi H, Akuta K. Vascular dilatation in the pelvis: identification with CT and MR imaging. Radiographics. 2004;24(1):193-208.
25. Naik A, Mian T, Abraham A, Rajput V. Iliac vein compression syndrome: an underdiagnosed cause of lower extremity deep venous thrombosis. J Hosp Med. 2010;5(7):E12-E13.
26. Lawenda BD, Mondry TE, Johnstone PA. Lymphedema: a primer on the identification and management of a chronic condition in oncologic treatment. CA Cancer J Clin. 2009;59(1):8-24.
27. O’Hearn DJ, Gold AR, Gold MS, Diggs P, Scharf SM. Lower extremity edema and pulmonary hypertension in morbidly obese patients with obstructive sleep apnea. Sleep Breath. 2009;13(1):25-34.
28. Blankfield RP, Zyzanski SJ. Bilateral leg edema, pulmonary hypertension, and obstructive sleep apnea: a cross-sectional study. J Fam Pract. 2002;51(6):561-564.
29. Berliner E, Ozbilgin B, Zarin DA. A systematic review of pneumatic compression for treatment of chronic venous insufficiency and venous
ulcers. J Vasc Surg. 2003;37(3):539-544.
30. Abbade LP, Lastória S, de Almeida Rollo H, Stolf HO. A sociodemographic, clinical study of patients with venous ulcer. Int J Dermatol. 2005;44(12):989-992.
31. Auzky O, Lanska V, Pitha J, Roztocil K. Association between symptoms of chronic venous disease in the lower extremities and cardiovascular risk factors in middle-aged women. Int Angiol. 2011;30(4):335-341.
32. Nelson EA, Mani R, Thomas K, Vowden K. Intermittent pneumatic compression for treating venous leg ulcers. Cochrane Database Syst Rev. 2011;(2):CD001899.
33. Pittler MH, Ernst E. Horse chestnut seed extract for chronic venous insufficiency. Cochrane Database Syst Rev. 2012;(11):CD003230.
34. Diehm C, Trampisch HJ, Lange S, Schmidt C. Comparison of leg compression stocking and oral horse-chestnut seed extract therapy in patients with chronic venous insufficiency. Lancet. 1996;347(8997):292-294.
35. Fitzpatrick TB, Wolf K, Johnson RA, Suurmond R, eds. Chronic venous insufficiency. In: Fitzpatrick’s Color Atlas & Synopsis of Clinical Dermatology. 5th ed. New York, NY: McGraw-Hill; 2005:475-479.
36. Fitzpatrick TB, Wolf K, Johnson RA, Suurmond R, eds. Atopic dermatitis. In: Fitzpatrick’s Color Atlas & Synopsis of Clinical Dermatology. 5th ed. New York, NY: McGraw-Hill; 2005:33-38.
37. Stanisic MG, Gabriel M, Pawlaczyk K. Intensive decongestive treatment restores ability to work in patients with advanced forms of primary and secondary lower extremity lymphoedema. Phlebology. 2012; 27(7):347-351.
38. Badger C, Preston N, Seers K, Mortimer P. Physical therapies for reducing and controlling lymphoedema of the limbs. Cochrane Database SystRev. 2004;(4):CD003141.
39. Adams KE, Rasmussen JC, Darne C, et al. Direct evidence of lymphatic function improvement after advanced pneumatic compression device treatment of lymphedema. Biomed Opt Express. 2010;1(1):114-125.
40. Ridner SH, McMahon E, Dietrich MS, Hoy S. Home-based lymphedema treatment in patients with cancer-related lymphedema or noncancerrelated lymphedema. Oncol Nurs Forum. 2008;35(4):671-680.
41. Kolbach DN, Sandbrink MW, Hamulyak K, Neumann HA, Prins MH. Non-pharmaceutical measures for prevention of post-thrombotic syndrome. Cochrane Database Syst Rev. 2004;(1):CD004174.
42. Kahn SR. Post-thrombotic syndrome after deep venous thrombosis: risk factors, prevention, and therapeutic options. Clin Adv Hematol Oncol. 2009;7(7):433-435.
43. Prandoni P, Kahn SR. Post-thrombotic syndrome: prevalence, prognostication and need for progress. Br J Haematol. 2009;145(3):286-295.
44. Enden T, Haig Y, Kløw NE, et al. Long-term outcome after additional catheter-directed thrombolysis versus standard treatment for acute iliofemoral deep vein thrombosis (the CaVenT study): a randomised controlled trial. Lancet. 2012;379(9810):31-38.
45. Makani H, Bangalore S, Romero J, Wever-Pinzon O, Messerli FH. Effect of renin-angiotensin system blockade on calcium channel blockerassociated peripheral edema. Am J Med. 2011;124(2):128-135.
46. Makani H, Bangalore S, Romero J, et al. Peripheral edema associated with calcium channel blockers: incidence and withdrawal rate—a metaanalysis of randomized trials. J Hypertens. 2011;29(7):1270-1280.
47. Birklein F. Complex regional pain syndrome. J Neurol. 2005;252(2):131-138.
48. Blankfield RP, Ahmed M, Zyzanski SJ. Effect of nasal continuous positive airway pressure on edema in patients with obstructive sleep apnea. Sleep Med. 2004;5(6):589-592.SORT: KEY



This clinic offers a calm and welcoming environment that immediately puts patients at ease. The dermatologist’s attention to detail and genuine concern for patient outcomes make every visit worthwhile. It is easy to see why this clinic has earned a reputation as the Best Dermatologist in Bangalore. Best Dermatologist in Bangalore
ResponderEliminar